Kurzprofil
Obgemsa® (Vibegron) ist ein hochselektiver β3-Agonist zur symptomatischen Behandlung der überaktiven Blase (ÜAB) bei Erwachsenen1.
β3-Agonisten führen zur Relaxation der Detrusormuskulatur in der Speicherphase, was die Blasenkapazität erhöht. Vibegron wirkt hochselektiv auf die für die Behandlung der ÜAB relevanten β3-Rezeptoren, hingegen nicht bzw. kaum auf β1- und β2-Rezeptoren2.
Vibegron wird bereits seit Jahren in den USA, in Südkorea und Japan bei ÜAB eingesetzt3,4.
ÜAB = überaktive Blase
REF:
1. Fachinformation Obgemsa, 01/25.
2. Brucker BM et al. Selectivity and Maximum Response of Vibegron and Mirabegron for β3-Adrenergic Receptors. Curr TherRes Clin Exp.2022 May 14:96:100674.
3. FDA Drug Trial Snapshot: Gemtesa. https://www.fda.gov/drugs/drug-approvals-and-databases/drug-trials-snapshot-gemtesa. Zugriff: 12.06.2024.
4. CHMP-Statement, Pierre Fabre Pharma. Data on file, April 2024.
Dosierung & Arzneimittelwechselwirkungen
Vibegron Filmtabletten 75 mg werden einmal täglich eingenommen. Die Tabletten könnten mit oder ohne Mahlzeiten eingenommen werden1.
Die Filmtabletten können auch zerkleinert, mit einem Esslöffel (ungefähr 15 ml) weicher Nahrung (z. B. Apfelmus) gemischt und unverzüglich mit einem Glas Wasser eingenommen werden1. Vibegron verursacht keine CYP2D6-Arzneimittelwechselwirkungen3.
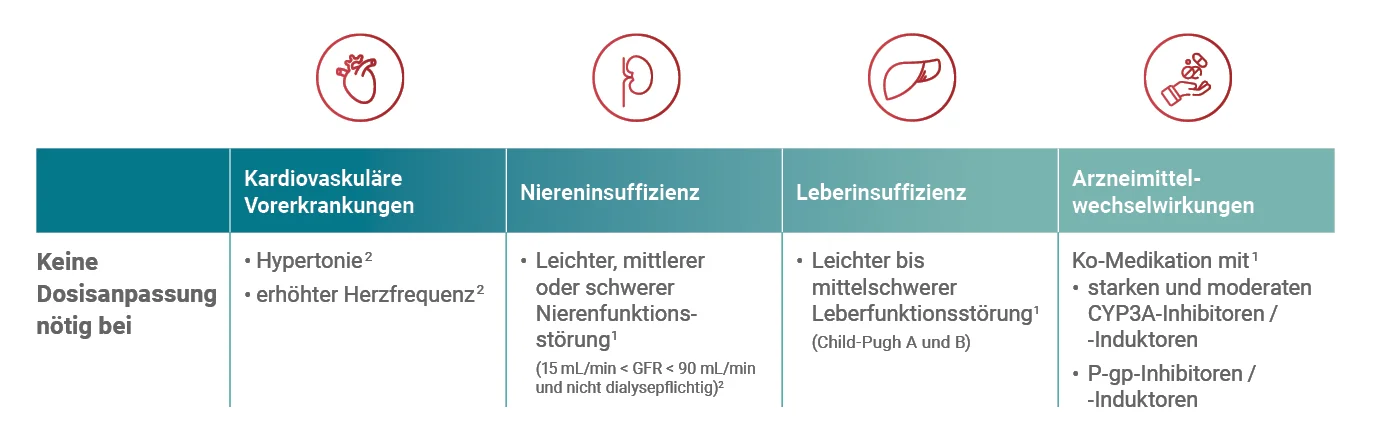
Vibegron wird nicht empfohlen bei Niereninsuffizienz im Endstadium sowie schwerer Leberschädigung (Child-Pugh C), bei Harnverhalt, in Schwangerschaft und Stillzeit sowie bei Kindern und Jugendlichen1.
Bei Ko-Medikation mit P-gp-Substrat Digoxin: Serumkonzentration überwachen, insbesondere bei Ko-Medikation mit P-gp-Substraten mit enger therapeutischer Breite (z. B. Dabigatranetexilat, Apixabanoder Rivaroxaban).

ÜAB-Patientinnen und Patienten leiden häufig unter weiteren Komorbiditäten wie z.B. BPH, Hypertonie oder Depression4 und nehmen entsprechend weitere Medikamente ein – viele von diesen werden über CYP2D6 verstoffwechselt:
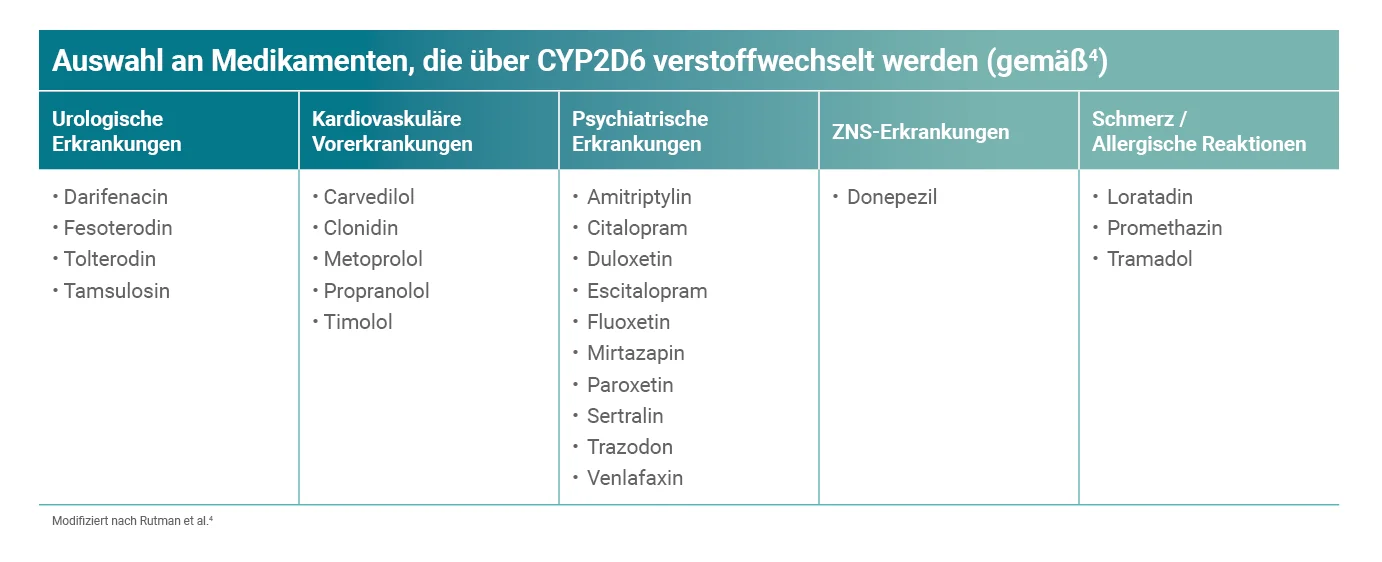
BPH = Benigne Prostatahyperplasie, ÜAB = überaktive Blase, ZNS = Zentrales Nervensystem
REF:
1. Fachinformation Obgemsa, 01/25.
2. Weber MA et al. Effects of vibegron on ambulatory blood pressure in patients with overactive bladder: results from a double-blind, placebo controlled trial. Blood Pressure Monitoring 2022;27(2):128-134.
3. Staskin D et al. Once-Daily Vibegron 75 mg for Overactive Bladder: Long-Term Safety and Efficacy from a Double-Blind Extension Study of the International Phase 3 Trial (EMPOWUR). J Urol.2021 May;205(5):1421-1429.
4. Rutman MP et al. Overactive Bladder Prescribing Considerations: The Role of Polypharmacy, Anticholinergic Burden, and CYP2D6 Drug‒Drug Interactions. Clin Drug Investig. 2021 Apr;41(4):293-302.
Darreicherungsformen
Vibegron 75 mg Filmtabletten
- Packungsgröße: 30 Stk. / PZN: 19171106
- Packungsgröße: 90 Stk. / PZN: 19171112
Obgemsa 75 mg Filmtabletten
Wirkst.: Vibegron. Zus.: 1 Filmtabl. enth. 75 mg Vibegron. Sonst. Bestandteile mit bekannter Wirkung: 1,5 mg Lactose. Sonstige Bestandteile: Tablettenkern: Mannitol, mikrokristalline Cellulose, Croscarmellose-Natrium, Hydroxypropylcellulose, Magnesiumstearat. Filmüberzug: Indigokarmin-Aluminiumsalz (E132), Hypromellose (E464), Eisen(III)-hydroxid-oxid x H2O (E172), Lactose-Monohydrat, Titandioxid (E171), Triacetin. Anwend.: Bei Erw. zur symptomat. Therapie bei überaktiver Blase (ÜAB-Syndrom). Gegenanz.: Überempfindlichkeit gegen Inhaltstoffe. Nebenw.: Häufig: Kopfschmerzen, Obstipation, Diarrhoe, Übelkeit, Harnwegsinfektion, Restharn erhöht. Gelegentl.: Hitzewallung, Ausschlag (einschließl. Ausschlag mit Juckreiz und erythematöser Hautausschlag), Harnverhalt (einschließl. Anstrengen beim Wasserlassen). Warnhinw.: enth. Lactose. Verschreibungspflichtig. Stand: Januar 2025.
DE-OBS-08-24-2400003